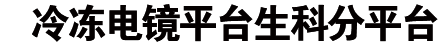江峰/金奇发现PVC作为新发人类致病的非共生发光杆菌的重要致病源
日期:2021-07-05 | 点击量:
非共生发光杆菌(Photorhabdus asymbiotica)是发光杆菌属(Photorhabdusspp.)中唯一被发现能导致人类感染的种类,但是对其致病机制人们却了解很少。Photorhabdus virulence cassette(PVC)代表一类广泛分布于细菌和古细菌中的细胞外可收缩注射系统(Contractile Injection Systems)。细菌中许多结构如六型分泌系统T6SS及R-type pyocins等均属于此类装置,它们被认为在细菌致病性中扮演了十分重要的角色。
近日,中国医学科学院病原生物学研究所
金奇课题组在
Science China Life Sciences发表了题为“
Characterization ofPhotorhabdusVirulence Cassette as a causative agent in the emerging pathogenPhotorhabdus asymbiotica
”的研究论文,阐明了PVC作为新发人类致病的非共生发光杆菌重要致病源的作用机制。
在前期的工作中,金奇研究员课题组与合作单位首次报导了一个完整PVC复合物的冷冻电镜结构(Cell, 2019),随后发现了PVC的一个效应蛋白RRSPPa能够通过抑制CDK1的磷酸化水平影响细胞增殖(Front. Microbiol.2020),然而效应蛋白是如何被装配进PVC以及PVC对何种类型宿主细胞直接发挥作用却仍未可知。此项研究中,进一步发现PVC的两个效应蛋白Pdp1和Pnf能够通过一种类似于“豌豆-豆荚”的方式被塞进PVC的内筒空间中,进而直接转运至哺乳动物巨噬细胞中发挥毒性作用。其中,Pdp1蛋白属于广泛存在的一类具有双重定位的dNTP焦磷酸酶(pyrophosphatase),具有一个DxDxxD活性位点。它在细胞核和微管中均有分布,通过降解细胞中的dNTP来影响细胞活性。Pnf则是一类脱酰胺酶(deamidase),通过对胞内Rho-GTPases(RhoA,Rac1,Cdc42)的脱氨基作用影响细胞骨架的形成,并最终导致细胞死亡。
广泛分布的Pdp1是具有哺乳动物细胞双重定位的dNTP焦磷酸酶效应蛋白
该研究不仅阐明了两个PVC效应蛋白Pdp1及Pnf的的装配方式,而且揭示了它们的作用机理以及PVC装置的直接作用对象。为后续深入理解非共生发光杆菌的致病机制和对PVC的改造利用奠定了坚实的基础。
中国医学科学院病原生物学研究所 王霞及北京大学生命科学学院 程稼萱为该文章的共同第一作者, 江峰副研究员和 金奇研究员为共同通讯作者。
原文链接:https://link.springer.com/article/10.1007/s11427-021-1955-4